Chemischer Wasserstoffspeicher
Physik-News vom 12.03.2019
Reversibles flüssigorganisches Wasserstoffspeichersystem aus einfachen organischen Chemikalien.
Wasserstoff ist ein leistungsfähiger, aber auch höchst explosiver Energieträger. Gesucht werden daher kostengünstige, leichte und vor allem sichere Speicher- und Transportsysteme. Wissenschaftler am Weizmann Institute of Science in Israel haben jetzt aus einfachen und ungefährlichen organischen Substanzen einen chemischen Wasserstoffspeicher entwickelt. Wie sie in der Zeitschrift Angewandte Chemie schreiben, zeichnet sich dieser flüssige Wasserstoffträger durch eine hohe theoretische Kapazität aus. Der gleiche Katalysator unterstützt die Wasserstoffladung und -entladung.
Wasserstoff enthält eine Menge Energie, die in elektrischen Strom umgewandelt werden kann. Als einziges Nebenprodukt bei der Verbrennung fällt Wasser an. Allerdings ist die Energiedichte pro Volumen des gasförmigen Wasserstoffs gering. Daher transportiert und speichert man Wasserstoff in der Regel unter Druck oder in flüssiger Form in schweren Stahlbehältern. Außerdem ist der Umgang mit Wasserstoff gefährlich.
Außer unter Druck kann Wasserstoff auch chemisch gespeichert werden. Er liegt dann, wie es die Natur vormacht, chemisch „maskiert” vor. In der biologischen Zelle binden sehr genau aufeinander abgestimmte chemische Komponenten den Wasserstoff und setzen ihn gezielt zum Aufbau chemischer Substanzen frei. Sämtliche Prozesse nutzen Enzyme als Katalysatoren.
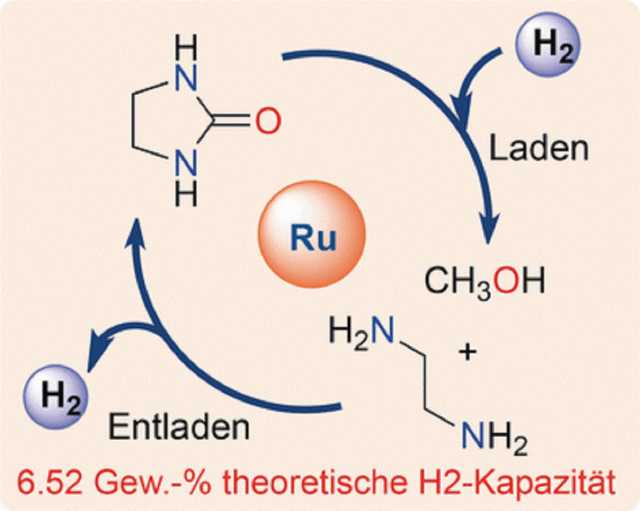
Auch in chemischen Laboratorien wurden leistungsfähige Katalysatoren entwickelt, um Wasserstoff umzusetzen, zum Beispiel den Ruthenium-Pinzettenkatalysator. Er besteht aus dem Schwermetall Ruthenium, das durch einen organischen Liganden löslich gemacht und für die Katalyse aktiviert wird. Mit diesen Katalysatoren untersuchten David Milstein und seine Kollegen, inwieweit einfache organische Chemikalien Wasserstoff speichern und freisetzen können.
„Ein geeignetes Wasserstoffspeichersystem ist nicht so einfach zu finden. Für die Wasserstoffwirtschaft ist es aber unerlässlich”, erklärten die Autoren ihre Motivation. Es muss aus ungefährlichen Chemikalien bestehen, einfach zu laden und entladen sein und so wenig Raum wie möglich einnehmen.
Milstein und Kollegen identifizierten Ethylendiamin und Methanol als einfach zu handhabende Grundchemikalien für ein solches System. Die Moleküle reagieren miteinander und setzen dabei Wasserstoff frei. Außerdem entsteht ein Produkt namens Ethylenharnstoff. Dieser „flüssigorganische Wasserstoffträger” (liquid organic hydrogen carrier, LOHC) hat eine für ein LOHC hohe theoretische Kapazität von 6.52 Gewichtsprozent.
Zuerst entwickelten die Wissenschaftler die Hydrierungsreaktion, also den Ladevorgang. Mit einem Umsatz von hundert Prozent reagierten Ethylenharnstoff und Wasserstoffgas zu den flüssigen Wasserstoffträgern Ethylendiamin und Methanol. Die Reaktion katalysierte der Ruthenium-Pinzettenkatalysator.
Dann untersuchten die Forscher die Entladung, also die Reaktion von Ethylendiamin mit Methanol. Hier betrug die Wasserstoffausbeute nahezu hundert Prozent, aber die Reaktion verlief über Zwischenprodukte. Am Ende stand ein Produktgleichgewicht. Weil die Produkte sich aber wieder vollständig hydrieren, also mit Wasserstoff beladen ließen, charakterisierten die Autoren ihr System als einen vollständig wieder aufladbaren chemischen Wasserstoffspeicher. Er besteht aus leicht zugänglichen, sicher handhabbaren und preisgünstigen flüssigen organischen Substanzen.
Vorteile sind seine Einfachheit und die hohe theoretische Kapazität. Er muss aber noch effizienter und „grüner“ werden, das heißt kürzere Lade-Entladezeiten und niedrigere Temperaturen bekommen. Vielleicht ließe sich das auch mit „grüneren” Katalysatoren erreichen.
Diese Newsmeldung wurde via Informationsdienst Wissenschaft erstellt.